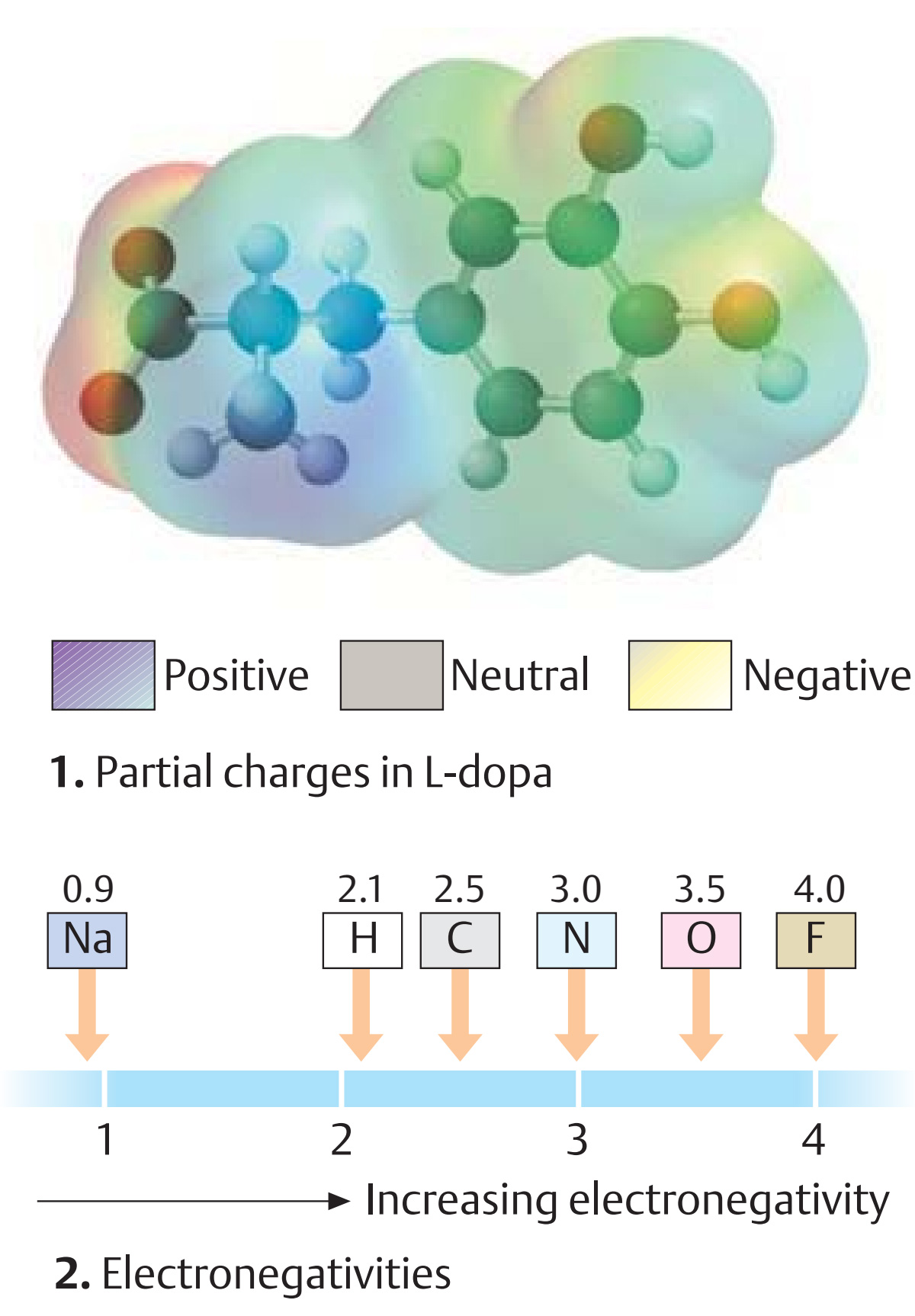
قطبیت باندها
بسته به موقعیت عنصر درجدول تناوبی ، اتم ها دارای الکترونگاتویته مختلف هستند ، که تمایل به گرفتن الکترونهای اضافی متفاوت هستند . مقادیر داده شده در C2 در مقیاس بین 2 تا 4 است.هرچه مقدار بیشتر باشد ، اتم الکتروناتیو تر می شود. هنگامی که دو اتم با بسیار الکترونگاتویته مختلف محدود به یکدیگر ، الکترونهای پیوندی کشیده می شوندبه سمت اتم الکترونگاتیو تر ، وپیوند قطبی است. اتمها درگیر هستندسپس جزئی یا مثبت یا منفی را تحمل کنید اتهامات در C1 سطح ون در والس استبا توجه به شرایط مختلف بار (رنگ قرمز = منفی ، آبی = مثبت) رنگی می شود. اکسیژن قویترین الکترونگاتیو است عناصر بیوشیمیایی مهم ، با C = O باند دو برابر به ویژه بسیار قطبی است.
Bond polarity
Depending on the position of the element inthe periodic table , atoms havedifferent electronegativity—i. e., a differenttendency to take up extra electrons. The values given in C2 are on a scale between 2 and 4.The higher the value, the more electronegative the atom. When two atoms with verydifferent electronegativities are bound toone another, the bonding electrons are drawntoward the more electronegative atom, andthe bond is polarized. The atoms involvedthen carry positive or negative partialcharges. In C1, the van der Waals surface iscolored according to the different charge conditions (red = negative, blue = positive). Oxygen is the most strongly electronegative of thebiochemically important elements, with C=Odouble bonds being especially highly polar.